Тема урока: Строение и свойства кристаллических тел.
Цели урока: Познакомить учащихся с правильной формой кристаллов и со свойством анизотропии, методом моделирования в изучении свойств кристаллов.
Дать школьникам представление о пространственной кристаллической решетке.
Показать ученикам на моделях разные типы Кристаллических решеток, взаимосвязь структуры кристалла и его свойств (механических, тепловых, электрических, оптических).
С целью патриотического воспитания познакомить школьников с ролью отечественных ученых в разработке физики твердого тела.
С целью политехнического образования показать значение физики твердого тела для народного хозяйства.
Методы обучения: Беседа. Рассказ. Демонстрация опытов. Работа с научно-популярной литературой. Моделирование. Наблюдения. Выдвижение гипотезы.
Оборудование. Демонстрационное: образование кристаллов, модель пространственной решетки кристаллов, модель, иллюстрирующая образование кристаллов и явление анизотропии, таблица «Кристаллы». Лабораторное: коллекция минералов и горных пород, выпускаемая для кабинета химии. Набор кристаллических и аморфных тел.
Литература: 1. Мякишев Г.Я., Буховцев Б.Б. Физика 10 кл. – М.: Просвещение 1992.
2. Тарасов Л. В. Этот удивительно симметричный мир. — М.: Просвещение, 1982.
3. Школьникам о современной физике: физика сложных систем. — М.1 Просвещение, 1978.
4. Энциклопедический словарь юного физика.
5. В.Г. Разумовский, Л.С. Хижнякова. Современный урок физики в средней школе. – М.: Просвещение, 1983.
6. Методика преподавания физики в 8 – 10 классах средней школы. Ч. 2/ Под ред. В.П. Орехова, А.В. Усовой и др. – М.: Просвещение 1980.
Структура урока: 1. Организационный момент………………….….2 мин.
2. Изложение и закрепление нового материала………..40 мин.
Переход вещества из газообразного состояния в жидкое, а затем в твердое.
Форма кристаллов.
Симметрия кристаллов.
Пространственная решетка.
Анизотропия монокристаллов.
3. Задание на дом………………………………………..3 мин.
Ход урока.
1. Организационный момент.
Учитель. Большинство окружающих нас твердых тел представляют собой вещества в кристаллическом состоянии. К ним относятся строительные и конструкционные материалы: различные марки стали, всевозможные металлические сплавы, минералы и т. д. Специальная область физики—физика твердого тела — занимается изучением строения и свойств твердых тел. Эта область физики является ведущей во всех физических исследованиях. Она составляет фундамент современной техники.
В любой отрасли техники используются свойства твердого тела: механические, тепловые, электрические, оптические и т. д. Все большее применение в технике находят кристаллы. Вы, наверное, знаете о заслугах советских ученых — академиков, лауреатов Ленинской и Нобелевской премий А. М. Прохорова и Н Г Басова в создании квантовых генераторов. Действие современных оптических квантовых генераторов — лазеров — основано на использовании свойств монокристаллов (рубина и др.). Как устроен кристалл? Почему многие кристаллы обладают удивительными свойствами? Каковы особенности структуры кристаллов, которые отличают их от аморфных тел? Ответы на эти и аналогичные вопросы вы сможете дать в конце урока. Запишем тему «Строение и свойства кристаллических тел»

Изложение и закрепление нового материала.
Обратимся к материалу прошлых уроков. Как вещество из газообразного состояния можно перевести в жидкое?
Ученик А. Чтобы вещество перевести из газообразного состояния в жидкое, надо газ охладить и сжать. Если охладить водяные пары до 0 °С, то они могут перейти в кристаллическое состояние — лед. При определенной температуре вещество из газообразного состояния переходит в жидкое, а затем при дальнейшем охлаждении оно испытывает еще одно превращение: жидкость переходит в твердое тело.
Учитель. Что происходит с веществом при его переходе из газообразного состояния в жидкое?
Ученик Б. Когда газ превращается в жидкость, его молекулы сближаются настолько, что среднее расстояние между ними становится в несколько раз меньше, чем в газе. Поэтому плотность жидкости во много раз больше плотности газа.
Учитель. Верно. В жидкости среднее расстояние между молекулами становится на порядок меньше (примерно в 10 раз), чем в газе. Соответственно плотность жидкости на три порядка больше (почти в 1000 раз) плотности газа.
Как вы считаете, не сводится ли отвердевание к такому же процессу? Быть может, при отвердевании молекулы сближаются еще больше?
Ученик В. Плотность вещества в твердом состоянии очень мало отличается от плотности того же вещества в жидком состоянии. В некоторых случаях даже плотность в твердом состоянии меньше, чем в жидком. Например, лед не тонет в воде, так как плотность его меньше плотности воды. Поэтому жидкость превращается в твердое тело не в результате сближения молекул.
Учитель. Молодец. Твоя догадка правильная. В твердом теле расстояние между молекулами такое же, как в жидкости. Как объяснить различие свойств твердых тел и жидкостей?
При одном и том же среднее расстоянии частицы в телах могут располагаться относительно друг друга по-разному. Однако существует такое взаимное расположение частиц, при котором каждая из них будет находиться в состоянии устойчивого равновесия. В твердом кристаллическом теле небольшие группы молекул или атомов (назовем их частицами) объединяются, образуя определенную фигуру. При этом они приходят в устойчивое равновесие. Вспомним условия, при которых тело (частица) будет находиться в устойчивом состоянии.
Ученик Г. Равновесие тела будет устойчивым, если при небольшом отклонении от этого положения силы, действующие на тело, возвращают его в первоначальное положение.
Учитель. Кто дополнит ответ?
Ученик Б. В положении устойчивого равновесия сумма сил, действующих на тело, равна нулю и потенциальная энергия тела минимальна.
Учитель. Твердое тело отличается от жидкости именно тем, что его частицы находятся в положении устойчивого равновесия. Частицы жидкости тоже могли бы расположиться так, чтобы положение каждой из них стало бы устойчивым. Однако этому мешает беспорядочное тепловое движение. Если понизить температуру, то средние скорости теплового движения уменьшатся и частицы займут устойчивое положение с минимальной потенциальной энергией. Именно это и происходит при отвердевании жидкости.
Перед вами на столах лежат наборы минералов и горных пород. Чем они
отличаются по внешнему виду?
Ученик А. Это кристаллические тела. Кристаллы одного и того же вещества имеют разнообразную форму. Углы между отдельными гранями кристаллов одинаковы. Некоторые формы кристаллов симметричны. Цвет кристаллов различен, — очевидно, это зависит от примесей.
Учитель. Кристаллы одного и того же вещества имеют разнообразную форму. Вы наблюдательны и правильно подметили свойства кристаллов. Большинство окружающих нас твердых тел — поликристаллы (сталь, чугун и др.). Они состоят из множества кристаллов, беспорядочно ориентированных друг относительно друга. Если вы внимательно посмотрите на минералы, то увидите отдельные кристаллы. Крупные одиночные кристаллы, имеющие правильную форму (обращается к таблице «Кристаллы»), в природе встречаются редко. Но такой кристалл можно вырастить в искусственных условиях. Посмотрите рост кристаллов. (Учитель демонстрирует опыт.) Обратите внимание, что для демонстрации роста кристаллов берется насыщенный раствор, например гипосульфита. Его охлаждают, и он становится пересыщенным. Достаточно в него поместить мельчайшие частицы кристалла, и раствор начинает кристаллизоваться. Если бы мы в течение всего времени кристаллизации поддерживали одинаковую температуру и плотность раствора во всем объеме, то кристалл в процессе роста принял бы правильную форму. В нашем опыте на форму кристалла влияют конвекционные потоки жидкости, наличие примесей и т. д. Поэтому кристаллы растут в виде причудливых совокупностей игл. Яркую и красочную картину вы наблюдаете благодаря приставки, позволяющей видеть рост кристаллов в поляризованном свете (проекция на потолок).
Идеальная форма кристалла имеет вид многогранника. Такой кристалл ограничен плоскими гранями, прямыми ребрами и обладает симметрией. В кристаллах можно найти различные элементы симметрии (показывает на таблице, где изображены кристаллы). плоскость симметрии, ось симметрии, центр симметрии. Например, кристаллы в форме куба (МаС1, КС1 и др.) имеют девять плоскостей симметрии, три из которых проходят параллельно граням куба, а шесть — по диагоналям. Кристаллы алмаза, калиевых квасцов имеют форму октаэдров. У кристаллов магния форма гексагональной призмы, т е. такой, которая опирается на правильный шестиугольник. Эти кристаллы обладают разной симметрией. На первый взгляд кажется, что число видов симметрии может быть бесконечно большим. В 1867 г. русский инженер А. В. Гадолин впервые доказал, что кристаллы могут обладать лишь 32 видами симметрии.
Симметрия кристаллов и другие их свойства, о которых мы будем говорить далее, привели к важной догадке о закономерностях в расположении частиц, составляющих кристалл. Может кто-нибудь из вас попытается ее сформулировать?
Ученик В. Частицы в кристалле располагаются так, что они образуют определенную правильную форму, решетку.
 Учитель. Частицы в кристалле образуют правильную пространственную решетку.
Пространственные решетки различных кристаллов различны. Перед вами модель
пространственной решетки поваренной соли. (Демонстрирует модель.) Шарики
одного цвета имитируют ионы натрия, шарики другого цвета — ионы хлора. Если
соединить эти узлы прямыми линиями, то образуется пространственная решетка,
аналогичная представленной модели. В каждой пространственной решетке можно
выделить некоторые повторяющиеся элементы ее структуры, иначе говоря
элементарную ячейку.
Учитель. Частицы в кристалле образуют правильную пространственную решетку.
Пространственные решетки различных кристаллов различны. Перед вами модель
пространственной решетки поваренной соли. (Демонстрирует модель.) Шарики
одного цвета имитируют ионы натрия, шарики другого цвета — ионы хлора. Если
соединить эти узлы прямыми линиями, то образуется пространственная решетка,
аналогичная представленной модели. В каждой пространственной решетке можно
выделить некоторые повторяющиеся элементы ее структуры, иначе говоря
элементарную ячейку.
 К наиболее простым элементарным ячейкам относятся куб, объемоцентрированный
куб, гранецентрированный куб, гексагональная призма. (Показывает на
таблице.) Понятие о пространственной решетке позволило объяснить свойства
кристаллов. Предсказание о структуре кристаллов было высказано Е. С.
Федоровым в 1890 г. В это время не существовало доказательств этой гипотезы,
даже существование молекул и атомов вещества многими ставилось под сомнение.
Такое предвидение строения кристаллов оставалось гипотезой до 1912 г., пока
не стали использовать рентгеновские лучи для исследования строения
кристаллов. Перед вами рентгенограмма кристалла. По ее виду можно
догадаться, что в расположении частиц в кристалле есть определенная
закономерность. Эти исследования подтвердили структуру пространственных
решеток кристаллов.
К наиболее простым элементарным ячейкам относятся куб, объемоцентрированный
куб, гранецентрированный куб, гексагональная призма. (Показывает на
таблице.) Понятие о пространственной решетке позволило объяснить свойства
кристаллов. Предсказание о структуре кристаллов было высказано Е. С.
Федоровым в 1890 г. В это время не существовало доказательств этой гипотезы,
даже существование молекул и атомов вещества многими ставилось под сомнение.
Такое предвидение строения кристаллов оставалось гипотезой до 1912 г., пока
не стали использовать рентгеновские лучи для исследования строения
кристаллов. Перед вами рентгенограмма кристалла. По ее виду можно
догадаться, что в расположении частиц в кристалле есть определенная
закономерность. Эти исследования подтвердили структуру пространственных
решеток кристаллов.
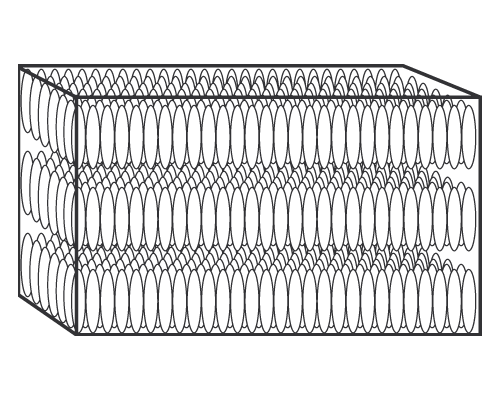
Посмотрите на лист слюды. Он легко расщепляется по плоскости (демонстрирует) и в то же время обладает высокой прочностью в направлении, перпендикулярном плоскости листа. И еще. Вспомните причудливые ледяные узоры на окнах. Форма снежинок свидетельствует о том, что кристаллизация паров воды в переохлажденном воздухе идет быстрее в определенных направлениях. Опыт со слюдой, наблюдение роста снежинок показывают, что свойства монокристаллов в разных направлениях неодинаковы. Можно указать и другие свойства, например теплопроводность, сопротивление, которые тоже зависят от направления по отношению к прямым, соединяющим узлы решеток. Эго свойство монокристаллов называют анизотропией. Перед вами гипс и стекло, гипс— кристаллическое тело, стекло — аморфное, в обычном состоянии оно не имеет кристаллической структуры, Подогреем их и покроем тонким слоем парафина, слегка проводя им по нагретым поверхностям гипса и стекла. (демонстрирую опыт.) Теперь раскаленной иглой прикоснемся к поверхности гипса. Аналогичный опыт проделаем с пластинкой стекла. (демонстрируется опыт с помощью проекционного аппарата). Что мы видим? Парафин расплавился. В опытах с гипсом на экране мы видим эллипс, а со стеклом — круг. Какой вывод можно сделать из этого опыта?
Ученик Б. Кристаллический гипс обладает свойством анизотропии теплопроводности, поэтому парафин на пластинке гипса плавится по различным направлениям неодинаково. Здесь проявляется различие между кристаллическими и аморфными телами.
Учитель. Как, исходя из кристаллической структуры твердых тел, объяснить свойство анизотропии?
Ученик Г. На модели пространственной решетки хлористого натрия видно, что каждый ион натрия окружен шестью ионами хлора. Если по грани решетки выбрать одно из вертикальных или горизонтальных направлений, то можно заметить, что чередуются черные и белые шарики — ионы натрия и хлора. Если провести прямую линию по диагонали, то на ней окажутся только белые или только черные шарики. Значит, не все направления в кристалле равноправны по строению. Это и является причиной анизотропии.
Учитель. Правильно. За активное участие в работе на уроке, оригинальные ответы ставлю ученикам А., Б., В., Г. оценку 5.
Посмотрите опыт, иллюстрирующий образование анизотропии. Вы видите в проекции на стекле стальные шарики, моделирующие ионы в кристаллах. Если провести через центр прямые линии, то можно убедиться, как первая из них пройдет через 9 шариков, вторая — через 5, третья — через 3. На единицу длины прямых, принадлежащих к различным семействам, приходится неодинаковое количество атомов, но свойства кристаллов зависят от плотности размещения образующих их частиц. Поэтому анизотропия является следствием правильного чередования атомов в монокристаллах.
О применении кристаллов и некоторых интересных физических явлениях, связанных с кристаллами, можно прочитать в научно-популярных книгах и журналах. На ваших столах лежат книги с закладками на определенных страницах. Прочитай те отрывки из этих книг, а потом я выборочно опрошу вас. (После 12-минутного чтения проводится опрос.)
Ученик Д. Я расскажу о жидких кристаллах. Некоторые органические материалы при переходе из жидкого состояния в твердое имеют промежуточную структуру. Вещество в таком состоянии называют жидким кристаллом. Для жидких кристаллов характерна вытянутая структура молекул, которая приводит к анизотропии свойств. Жидкие кристаллы обладают важными оптическими свойствами, которые в широких пределах изменяются внешними воздействиями. Это и определяет большие возможности управления световыми потоками с помощью жидких кристаллов.
Учитель. Молодец. За работу с книгой ставлю оценку 5.
Ученик Е. Я расскажу о роли некоторых добавок в сплавы для увеличения прочности материалов, т. е. для упрочнения.
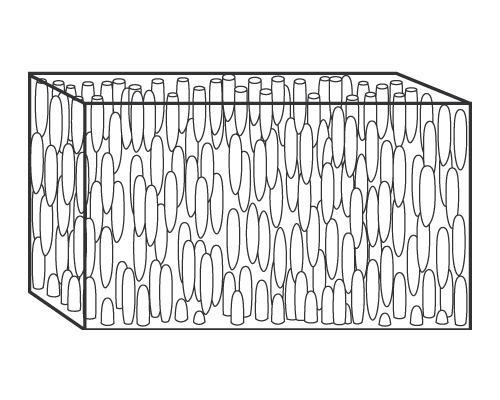 Правильное расположение атомов в кристаллах далеко не всегда идеально.
Размещение атомов в пространстве часто нарушается. Эти области
разупорядочения атомов кристаллической решетки называют дефектами. Иногда
нарушается правильная структура пространственной решетки вдоль некоторых
линий. Эти дефекты называются дислокациями. Обычно примеси в металлах
оседают на дислокации. Большое число примесей может полностью блокировать
дислокации. Сталь представляет собой сплав на основе железа, содержит
значительные примеси углерода, а также различные легирующие добавки (примеси
некоторых металлов). Регулируемое упрочнение стали, происходит за счет
взаимодействия атомов примеси, в том числе и углерода, с дислокациями и за
счет выпадения микроскопических включений карбида железа. В настоящее время
это основной путь упрочнения конструкционных материалов.
Правильное расположение атомов в кристаллах далеко не всегда идеально.
Размещение атомов в пространстве часто нарушается. Эти области
разупорядочения атомов кристаллической решетки называют дефектами. Иногда
нарушается правильная структура пространственной решетки вдоль некоторых
линий. Эти дефекты называются дислокациями. Обычно примеси в металлах
оседают на дислокации. Большое число примесей может полностью блокировать
дислокации. Сталь представляет собой сплав на основе железа, содержит
значительные примеси углерода, а также различные легирующие добавки (примеси
некоторых металлов). Регулируемое упрочнение стали, происходит за счет
взаимодействия атомов примеси, в том числе и углерода, с дислокациями и за
счет выпадения микроскопических включений карбида железа. В настоящее время
это основной путь упрочнения конструкционных материалов.
Учитель. Молодец. Вы усвоили материал урока и применили его к объяснению интересного технического явления, связанного с повышением прочности материалов. Оценка за ответ 5.
Ученик Ж. Я покажу на примере графита и алмаза, что свойства кристаллических веществ определяются структурой кристаллических решеток.
Между алмазом и графитом оказывается много общего, хотя на первый взгляд это общее трудно увидеть. Алмаз необычно тверд, прозрачен, не проводит электрический ток (диэлектрик), обработанные алмазы — драгоценность, известны в быту как бриллианты.
Графит мягок, легко расслаивается, непрозрачен, электропроводен и не похож на драгоценный камень. А между тем и алмаз, и графит — это чистый углерод. Различие свойств алмаза и графита связано только с различием кристаллических решеток. (Ученик показывает рисунок с изображением кристаллических решеток алмаза и графита.)
При определенных условиях возможен переход вещества из одной кристаллической
модификации в другую. Если нагреть графит до температуры 2000—2500 К под
давлением 1010 Па, то произойдет перестройка кристаллической
решетки, в ре зультате чего графит превратится в алмаз. Так получают
искусственные алмазы.
зультате чего графит превратится в алмаз. Так получают
искусственные алмазы.
Учитель. Вы сегодня хорошо работали на уроке, помогали проводить опыты. Ставлю вам оценку 5.
Ученик 3. Я расскажу о загадке воды: почему вода ведет себя иначе, чем другие жидкости при нагревании от 0 до 4 °С.
Известно, что плотность жидкостей, как правило, уменьшается при нагревании; их вязкость возрастает при увеличении внешнего давления. Вода является исключением. При нагревании от 0 до 4 °С плотность воды возрастает, ее вязкость с повышением давления уменьшается. Благодаря этому в водоеме подо льдом устанавливается температура 4 °С. Уплотнение воды при повышении температуры от 0 до 4 °С связано с тем, что при нагревании все чаще происходит разрыв межмолекулярных связей, в результате чего взаимное расположение молекул все больше напоминает плотную упаковку шаров. Уменьшение плотности воды при нагревании выше 4 °С объясняется тем, что этот эффект начинает подавляться другим, а именно эффектом теплового увеличения расстояний между атомами кислорода и водорода внутри молекул воды. Существование ажурной молекулярной структуры воды (при температуре, близкой к О °С) объясняется и уменьшением ее вязкости с увеличением внешнего давления. При повышении давления происходит разрыв межмолекулярных связей, что приводит к уменьшению вязкости.
Учитель. За обоснованный ответ и активную работу на уроке ставлю оценку 5.
Откройте дневники и запишите задание на дом: § 18; повторить § 29 («Физика-8»). Задание для желающих: вырастить кристаллы из раствора медного купороса или квасцов. Советую вам прочитать книги, отрывки из которых мы сегодня обсуждали.
Напишите мне: demkin-nik@yandex.ru ICQ: 276-807-301 E-mail школы: stshkola1@mail.ru